Minéralogie des gîtes minéralogie de la galène
La minéralogie des gîtes est une branche de la Géologie, qui étudie les minéraux des gîtes métallifères ; le minéral étant défini comme un corps inorganique formé suite à des combinaisons physico-chimiques d’éléments chimiques naturels dans l’écorce terrestre. Elle s’intéresse à la composition chimique des minéraux, à leurs propriétés physiques et chimiques, à leurs structures cristallines et à leurs genèses. Elle permet ainsi de déterminer exactement les minéraux, et de connaître leur milieu naturel et les lois de leur association. Analyse chimique Un minéral de galène est constitué d’un assemblage d’atomes ou d’ions de natures différentes, régi par divers processus liaisons atomiques, processus d’encombrement et phénomène de remplacement.
Composition chimique
La galène est un minéral métallique. Dans son état de pureté maximale, la galène est composée de 86.6 % de plomb (Pb) et 13.4 % de soufre (S) en masse ‘10’ ; cette proportion correspond à la composition stœchiométrique Pb1S1. Ainsi, une masse de 1 Kg de galène pure renferme les mêmes quantités de mole de plomb et de soufre, soit 4.17 moles (86.6/100) * (1000g/207.21g) = (13.4/100) * (1000g/32.1g) = 4.17 moles, mPb = 207.21 g et mS = 32.1 g étant respectivement les masses molaires du plomb et du soufre. Bref, la galène est un monosulfure de formule chimique PbS (Pb2+, S2-) et de poids moléculaire égal à 239.31 g . Dans la nature, outre ces principaux éléments chimiques (plomb et soufre), la galène contient également de métaux d’impureté sous forme d’inclusions chimiques • impureté utile, qui donne une valeur supplémentaire à la galène argent. Dans une première approche, sa présence est reconnue en dissolvant une masse pulvérisée de galène dans l’acide azotique (nitrique) HNO3 et en plongeant dans la liqueur obtenue (acide azotique + galène) une lame de cuivre bien décapée, qui se recouvre d’enduit d’argent ‘7’. L’analyse de cet enduit d’argent à la perle de borax donne une couleur jaune claire à chaud et une couleur jaune irisé à froid. On admet que la galène présentant de petites facettes est plus argentifère que celle à larges facettes ‘7’. Cette richesse en argent est en outre en relation avec la présence d’une roche encaissante calcaire ou contenant de la pyrite FeS2 ‘7’ . • impureté nuisible, qui gêne le traitement chimique et thermochimique ou nécessite de procédé supplémentaire d’élaboration de composés de plomb Plus de 10 % de zinc provoque une perte de plomb par volatilisation ‘6’ lors d’un traitement thermique de la galène car le zinc libère le plomb par substitution. Le bismuth est nuisible même à l’état de trace 0.01% de bismuth suffit à provoquer la corrosion ‘6’ du métal de plomb en s’associant avec celui-ci. La somme arsenic + étain + antimoine est refusée à 5 % ‘6’ pour cause d’impossibilité technique d’affinage. Dans tous les cas, le minéral est vendable dès la teneur de 55 % en plomb ‘6’ .
Liaison atomique régissant la combinaison d’atomes formant la galène
Plusieurs liaisons atomiques sont connues jusqu’à l’heure actuelle (liaison ionique, liaison covalente, liaison de Van Der Waals, liaison hydrogène et enfin liaison métallique). Parmi ces liaisons, la liaison métallique est caractéristique des métaux et elle régit la combinaison des atomes formant la galène principaux éléments constitutifs et éléments d’impureté. Les atomes formant la galène s’arrangent en un empilement compact baignant dans un nuage d’électrons. Ce nuage d’électrons maintient ces atomes les uns au contact des autres, qui se comportent comme des boules empilées et se déplacent les uns par rapport aux autres. Ce schéma explique la conductibilité thermique et électrique de la galène. Figure 1 Arrangement des principaux atomes de galène.pouvant être considérés comme des boules empilées.
Phénomène d’encombrement des atomes à l’intérieur du minéral de galène
Ce phénomène traduit le volume et la figure que dessinent les atomes de la galène par suite de la liaison métallique, décrite précédemment. Le principe est tel que deux atomes se rapprochent jusqu’à une certaine distance seuil (distance limite) égale à la somme des rayons ioniques correspondants. La figure obtenue en observant les sommets occupés par les atomes forment un polyèdre de coordinat. La forme et la taille du polyèdre sont déterminées par la coordinence (nombre d’atomes directement au contact d’un atome considéré) d’un atome principal (plomb ou soufre) pris arbitrairement comme référence ; la valeur de cette coordinence est égale à 6 pour chaque atome principal de la galène, et correspond à un cube. Outre le phénomène de remplacement, le paragraphe suivant traitera davantage cette notion.
Cristallographie géométrique
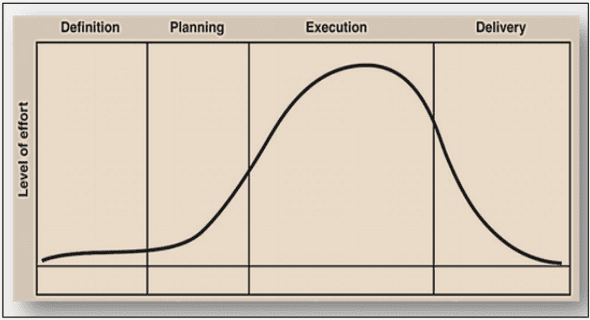
Cette approche sur la cristallographie de la galène doit déboucher aux connaissances des conséquences de la structure cristalline sur ses propriétés physiques. Ainsi, dans un premier temps, l’étude fournira des renseignements sur la description (structure, texture et morphologie) correcte et simple des empilements conduisant aux cristaux, puis expliquera les relations existant entre ces éléments d’information et les propriétés physiques du cristal de galène. Cristal de galène un cristal comme tant d’autres. Un cristal est défini comme une répétition périodique d’un groupe identique d’atomes dans les trois dimensions de l’espace. Cet état peut être schématisé en considérant ces atomes comme des boules occupant des points ou nœuds de l’espace, dont l’ensemble forme un réseau. Ce groupe élémentaire d’atomes forme ce qu’on appelle ‘une maille’. La galène construite suivant une structure et texture atomique Dans la nature, la galène se rencontre à l’état cristallin qui est caractérisé par l’arrangement régulier des atomes la constituant. En adoptant le principe de représentation des dispositions des atomes dans l’espace, énoncé dans le paragraphe précédent, cet arrangement régulier des atomes constituant la galène se traduit en une forme de cube à faces centrées les atomes de plomb se trouvent aux sommets des arêtes et au centre des faces, et ceux du soufre au milieu des arêtes et au centre de la maille cubique, d’où l’assertion ‘la galène cristallise dans le système cubique à face centrée (C.F.C.)’. Les nombres Z d’atomes de plomb et du soufre, correspondant à une maille cubique, sont égaux à quatre (4) chacun, c’est-à-dire, une maille est formée de Z = 4 molécules de PbS, constituées de 4 atomes de plomb et 4 atomes de soufre. La figure ci-après schématisant l’empilement des atomes de galène, représente les dispositions des atomes de plomb et de soufre, vues en perspective. Figure 2 Représentation schématique de l’empilement des atomes de plomb et de soufre dans un cristal de galène. représente les atomes de plomb aux sommets et centre des faces (1 atome de Pb / 8 mailles) * 8 sommets + (1 atome Pb / 2 mailles) * 6 faces = 4 atomes de Pb. représente les atomes de soufre aux milieux des arêtes et centre de la maille (1 atome de S / 4 mailles) * 12 arêtes + 1 atome de S au centre = 4 atomes de S. La disposition des atomes de plomb aux sommets et centres des faces forme un plan réticulaire. La taille d’une maille cubique est de l’ordre de 5.94 Å (Angtröm 1 Å = 10E -7 mm), donnant un volume égal à 210E -21mm3 . Possibilité de remplacement des atomes dans le réseau cristallin de la galène La présence des impuretés métalliques dans le réseau cristallin de la galène s’explique par le fait que les places qu’occuperaient normalement certains atomes de plomb dans l’état de pureté maximale de la galène, deviennent celles des impuretés métalliques à condition que les rayons ioniques de ces dernières soient, au plus, égaux à celui du plomb (le rayon de l’ion plombeux Pb2+ est égal à 1.32 Å avec une coordinence de 6 ‘8’) pour permettre le remplacement. Sous cette même restriction spatiale, les sites interstitiels octaédrique (Figure 3(a)) et tétraédriques (Figure 3(b)) laissés entre les atomes principaux (plomb et soufre) sont également des places disponibles pour les impuretés métalliques. Figure 3 Schéma de sites interstitiels octaédrique (a) et tétraédriques (b) dans le système C.F.C. Comportements physiques tirés des caractères cristallographiques de la galène • Forme en jeu de construction La galène se présente sous forme d’ensemble de cubes empilés et limités par des surfaces planes, qui constitue la manifestation macroscopique de cet état cristallin cubique interne les atomes de plomb et de soufre sont régulièrement disposés en dessinant des cubes empilés les uns sur les autres. • Clivages orthogonaux Le cristal de galène se fragmente suivant les trois plans principaux orthogonaux correspondant aux trois faces perpendiculaires du cube ; une face étant formée, entre autres, par les nœuds qu’occupent les atomes de plomb. • A l’échelle macroscopique, les plans réticulaires formés par les atomes de plomb (les atomes occupent les nœuds de la face plane du cube) sont matérialisés par le comportement de la surface de clivage comme un miroir plan optimisant la réflexion des rayons lumineux incident et intensifiant ainsi l’éclat métallique de ces atomes du plomb. • Du fait de l’état cristallin de la galène, la fusion de celle-ci intervient de façon franche à la température de fusion, par opposition au corps solide amorphe dont l’évolution de l’état solide à l’état liquide passe par une transition pâteuse pour arriver à l’état fluide de façon continue. Figure 4 Courbe d’évolution de l’état d’un cristal de galène au fur et à mesure de l’augmentation de la température. 2 – 3 représente le palier de discontinuité, pendant lequel la phase liquide et la phase solide (cristal de galène) coexistent ; le point 2 marque le solidus (apparition du premier liquide), tandis que le point 3 marque le liquidus (disparition du dernier solide). • De même, l’anisotropie, propriété caractéristique du cristal, peut être continue ou discontinue la galène, minéral métallique, est anisotropique de façon continue vis-à-vis de la conductivité électrique et thermique ; elle est anisotropique de façon discontinue vis-à-vis de fragmentation (cassure et clivage).
Identification au microscope métallographique (utilisant la lumière réfléchie)
Pouvoir réflecteur
Le pouvoir réflecteur est défini comme le rapport de l’intensité lumineuse réfléchie par une section à l’intensité lumineuse reçue par cette section. En se référant à l’assertion sur la réflexion de la lumière incidente sur un minéral de galène au niveau de sa surface de clivage, le pouvoir réflecteur y est distinctement observable il est de l’ordre de 42.5 %. Poli ou figure d’arrachement La galène présente un mauvais poli ou figure d’arrachement caractéristique, observable en lumière naturelle au microscope métallographique. Cette figure prend la forme de triangle d’arrachement. Figure 5 Schéma du poli de la galène au microscope métallographique. Identification à l’échelle macroscopique La galène possède des propriétés qui sont en liaison causale avec sa composition chimique et sa structure cristalline. Ces propriétés sont traduites en des indices particuliers qui la différencient des autres minéraux. Ainsi, la galène est identifiée très exactement d’après les particularités suivantes Morphologie du minéral • Hétérogénéité Le minéral de galène peut être qualifié par son aspect extérieur résultant du mode d’assemblage des cristaux à l’intérieur. Ainsi, il peut être bien développé (la taille atteignant 40 cm) ou se présente en masses très fines. • Forme isométrique Le minéral peut être caractérisé par sa forme cristalline extérieure ou ‘habitus’ ; Dans l’ensemble, le minéral de galène, qui apparaît comme une masse en jeu de construction, adopte la forme isométrique le minéral est également développé dans toutes les trois directions de l’espace. Cet état d’être bien développé est souvent désigné par le terme ‘automorphe’. • Opacité Le minéral peut être également caractérisé par son opacité qui est une propriété du minéral à ne pas laisser passer la lumière pour une épaisseur de couche de 1 cm. • Couleur gris bleuâtre Le minéral peut être également caractérisé par sa couleur ; la couleur gris bleuâtre de la galène semble tenir de la couleur gris bleuâtre du plomb. C’est donc un minéral idiochromatique, c’est-à-dire, la couleur du minéral est directement liée à sa composition chimique interne. • Eclat Il n’est pas surprenant d’observer un éclat métallique (caractéristique des minéraux métalliques) sur une facette clivée d’un minéral de galène à cause de la présence du plomb. Ainsi, la galène dont le pouvoir réflecteur est, rappelons-le, de 42.4 %, brille par son éclat métallique (aspect scintillant). • Clivages orthogonaux Le minéral peut être caractérisé par la façon dont il se brise ; il se sépare parfois en éléments semblables suivant des plans bien déterminés. Cette propriété est celle que nous avons désigné par le terme ‘clivage’ ; le plan du clivage est repéré par l’indice (h,k,l) de Miller. Les surfaces de clivage sont nettement observables, étant donné que la galène ne prend forme que suivant ces plans de clivage plans orthogonaux (1,0,0), (0,1,0), (0,0,1), donnant un aspect en escalier. En ce qui concerne la qualité du clivage, elle est parfaite le minéral se clive suivant des surfaces lisses et il est très difficile d’obtenir une fracture autre que suivant ces plans de clivage. Figure 6 Photographie d’un échantillon de minéral de galène, prélevé dans la région de Tsaratanàna. • Trait noir La couleur de la poussière ou de la poudre du minéral peut être un caractère valable de reconnaissance. Elle correspond à la couleur du minéral très finement divisé et est obtenue par frottement du minéral sur une plaque de porcelaine non-émaillée. La galène laisse une trace noire, et cet état nous prévient déjà sur la couleur des particules fines qui seront obtenues après sa fragmentation. Caractéristiques mesurables • Dureté Le minéral peut être caractérisé par sa résistance à la rayure, rapportée à l’échelle de Mohs la dureté s’apprécie par rapport à des minéraux étalons suivant que l’échantillon à tester raye ou est rayé par ces minéraux étalons Talc de dureté égale à 1 ; Gypse, 2 ; Calcite, 3. Pratiquement, certains objets courants servent d’étalons pour situer la dureté d’un minéral en référence avec l’échelle de Mohs ongle de dureté égale à 2.5 ; lame de verre, 5.5 ; acier dur (lime), 6.5. Rapportée sur l’échelle de Mohs, la dureté de la galène varie de 2.5 à 2.7 ‘10’. Pratiquement, sa facette n’est pas rayée par l’ongle, mais l’est avec une lame de verre ou un acier dur (lime). • Ténacité Le minéral peut être caractérisé par sa résistance à la coupure, à la cassure et au broyage (un minéral peut être tenace, cassant, ou tendre – le diamant est dur mais cassant –). Une masse de galène est facilement fragmentée en grains fins ; c’est un minéral tendre. Cet état nous prévient déjà de la facilité du broyage des cristaux de galène, outre la finesse de leurs structures dans un dépôt exogène. • Densité Le minéral peut être caractérisé par son poids spécifique mesuré à l’aide de pycnomètre. La galène possède une densité variant de 7.2 à 7.6 g/cm3 ‘10’; c’est un minéral très dense. D’ailleurs, jaugé à la main, cet état est déjà palpable. Propriétés et constantes physiques‘8’ • Magnétisme Le magnétisme est détecté par la sensibilité de l’aiguille aimantée en présence du minéral. Cette propriété permet de différencier les minéraux ferreux de tout le reste. L’aimant n’influe guère sur la galène. C’est une propriété intéressante car elle permet de distinguer, sans aucun doute, la galène de la magnétite ou de l’hématite (montrant également un éclat métallique). • Fusion Avec une chaleur de fusion égale à 1114 Cal / mole, le composé PbS fond vers 1100 °C suivant que – l’accroissement de la teneur en soufre élève ce point de fusion, – la présence d’impuretés diminue ce point de fusion vers 940 à 930 °C correspondant à la galène naturelle. Dans tous les cas, le composé PbS fond au rouge ; A une température supérieure au point de fusion, il se volatilise lentement au rouge blanc. A une température de 250 °C, la chaleur spécifique de la galène est égale à C = 0.04912 Cal / g.°C. • Conductibilité électrique et thermique ‘8’ Le matériau de galène possède la propriété de semi-conducteur électrique suivant qu’elle renferme une composition chimique qui s’écarte légèrement de la composition stœchiométrique idéale Pb1S1 ‘8’ – avec un excès de soufre, la galène se comporte comme un semi-conducteur de type p (positif) ; les atomes excédentaires de soufre (accepteur d’électrons) attirent des électrons libres. – avec un excès de plomb, la galène fonctionne comme un semi-conducteur de type n (négatif) ; les atomes de plomb donnent des électrons libres. En somme, l’existence de surface de contact de deux zones de type n et de type p au sein d’un même cristal de galène présente une conductibilité électrique très grande de la zone p vers la zone n, et très faible dans le sens inverse ; Pratiquement, un cristal de galène, renfermant de telle surface, conduit le courant dans un seul sens, et cette propriété est exploitée dans les composantes électroniques (redresseur de courant). La galène conduit moyennement la chaleur son coefficient de conductibilité thermique λ qui est égal à 570E -5 cal / cm². s . °C ‘7’ = 0.87 W/m².°K avoisine la valeur de référence de 1.3 W/m2.°K ‘19’ . Il y a lieu de noter que le coefficient de conductibilité thermique d’un matériau est la quantité de chaleur qui passe par seconde à travers 1 m² de la surface du matériau d’épaisseur déterminée pour une différence de température de 1 °K entre les milieux de part et d’autre du matériau. Méthode de reconnaissance méthode par voie sèche ‘7’ ET ‘8’ . Deux méthodes de reconnaissance sont généralement utilisées pour reconnaître l’identité d’un minéral méthode de reconnaissance par voie sèche et méthode de reconnaissance par voie humide. Cependant, la reconnaissance par voie sèche suffit pour trancher sur l’identité de la galène, d’autant plus qu’elle est réalisable avec un minimum de matériels (charbon de bois, tube en verre, poudre de borax, bec bunsen). La méthode par voie sèche utilise des matériaux spécialement traités, sur lesquels va être déposée une poudre du minéral à tester ; Exposé à la flamme de bec bunsen, l’ensemble (matériaux, poudre du minéral) forme des dépôts observables, caractéristiques pour chaque minéral. • Essai sur le charbon L’opération consiste à exposer à la flamme du bec bunsen (chalumeau) des poudrse du minéral à tester et de carbonate de sodium NaCO3 (un fondant), dans une proportion de 1 / 3, le tout déposé sur une fente spécialement conçue sur un tige de charbon de bois. La flamme change ce mélange de particules minérales en des boutons métalliques avec enduit jaune à contour blanc ce qui confirme qu’on est en présence d’un minéral de galène. • Essai à la perle de borax L’opération se déroule en deux phases – Préparation de la perle Cette phase consiste à chauffer à la flamme du bec bunsen l’extrémité d’un fil de silice, puis l’enfoncer immédiatement dans un amas de poudre de borax, et enfin la présenter de nouveau à la flamme. Une perle transparente va se former à cet endroit du fil. – Observation de la coloration caractéristique de la perle en présence de poudre du minéral à tester L’opération continue par un dépôt soigneux de poudre du minéral à tester sur la perle, puis une exposition de l’ensemble à la flamme. La perle prend alors une coloration caractéristique sous la flamme la présence de particules de galène est confirmée par l’obtention d’une coloration jaune claire à chaud, incolore à froid, au feu oxydant (partie supérieure bleue de la flamme), et d’une coloration grisâtre à chaud et à froid, au feu réducteur (noyau jaune de la flamme). • Essai en tube ouvert L’opération consiste à verser dans un tube de verre, courbé à 120°, une poudre de minéral à tester. L’ensemble est exposé à la flamme du bec de bunsen à l’endroit de la courbure où se concentre la poudre du minéral. A terme, un dépôt d’enduit blanc se forme parmi les particules pulvérulentes, confirmant la présence de poudre de galène.
PARTIE 1 COLLECTE ET ANALYSE DES ELEMENTS D’INFORMATIONS |