Télécharger le fichier original (Mémoire de fin d’études)
Fabrication des échantillons
Epitaxie
Les échantillons que nous avons utilisés comme « donneurs » pour la technologie Smart CutTM sont composés d’un substrat silicium de type p sur lequel est épitaxié un buffer de (typiquement) 200 nm de silicium intrinsèque puis une couche de 5 nm de Si:B ou de SiGe puis une couche de silicium de 100 nm. La structure est présentée en Figure 1.
Les couches ont été réalisées par dépôt chimique en phase vapeur (CVD) qui est une technique permettant de déposer des couches minces de diverses natures sur un substrat. Son principe est basé sur la décomposition d’un ou plusieurs précurseurs gazeux qui contiennent l’élément que l’on souhaite déposer [SIV95]. La décomposition des molécules permettant l’incorporation des atomes dans la couche a lieu par apport d’énergie. Cette énergie est généralement apportée en chauffant le substrat. De nombreuses variantes de ce type de procédé existent qui se différencient, par exemple, par les conditions de pression ou la présence d’un plasma ou non.
Dans notre cas, pour réaliser nos différentes couches, la technique d’épitaxie par RPCVD (Reduce Pressure Chemical Vapor Deposition) a été utilisée. Dans un réacteur RPCVD (cf. Figure 2), la pression typique dans l’enceinte est de l’ordre de la dizaine de Torr.
Le silane (SiH4), diborane (B2H6) et germane (GeH4) sont utilisés comme précurseurs pour, respectivement, le silicium, le bore et le germanium. L’épitaxie se réalise dans la gamme de températures 600°C – 750°C, par décomposition de ces espèces gazeuses entraînées par un gaz vecteur (ici, de l’hydrogène).
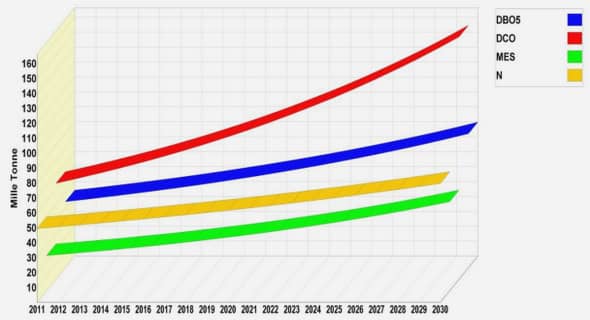
Les profils de concentration de B et Ge sont présentés en Figure 3. Ils montrent que les couches enterrées de Si:B et SiGe sont à environ 100 nm de profondeur (pic de B et de Ge), comme attendu. De plus, l’épaisseur de ces couches semble proche des 5 nm visés initialement (largeur à mi-hauteur du pic = 6 nm). La concentration de bore dans la couche est d’environ 1.1019 at/cm3, qui correspond au dopage visé. Par contre, la couche SiGe semble être composée d’un peu plus de germanium que prévu (environ 25% d’après le SIMS contre 20% visé). Globalement, nous pouvons dire que les couches épitaxiées correspondent à ce que nous attendions.
Oxydation thermique
Dans la technologie Smart CutTM, il est usuel que l’oxyde enterré soit réalisé par oxydation thermique de la plaque qui sera implantée. Cela présente l’avantage d’éloigner l’interface de collage, qui peut être défectueuse, de la couche active dans laquelle vont être réalisés les dispositifs. Cette oxydation a lieu à haute température (1050°C). Or, nous ne voulons pas exposer nos plaques à de tels bilans thermiques pour ne pas que le bore ou le germanium contenu dans la fine couche enterrée ne diffuse dans le reste du substrat.
Dans notre cas, nous réalisons donc l’oxyde, de 50 nm d’épaisseur, sur la plaque de silicium qui sera collée à la plaque implantée qui contient la couche enterrée.
Implantation ionique
Principe général
L’implantation ionique consiste à bombarder un matériau avec des ions de l’impureté désirée, accélérés à des énergies variant de quelques kilo-électronvolts (keV) à quelques mégaélectronvolts (MeV). Un ion énergétique pénétrant dans un substrat perd son énergie en partie par chocs nucléaires sur les atomes de la cible, déplaçant ces derniers et créant des défauts (lacunes et interstitiels) sur son parcours. En fin de parcours, l’ion incident s’immobilise sur un site interstitiel ou substitutionnel de la matrice.
La technique d’implantation ionique présente trois avantages majeurs :
– La distribution en profondeur des ions implantés dans le matériau est localisée et contrôlée par l’énergie du faisceau d’ions.
– La quantité totale d’ions introduits peut être mesurée par le courant généré par l’arrivée des particules chargées à la surface de l’échantillon.
– Enfin, il est possible d’introduire des concentrations d’impuretés au-delà de la solubilité limite d’une espèce dans le matériau et d’introduire des espèces qui ne peuvent pas être diffusées.
Pour avoir une vision exhaustive de la physique et de la technologie de l’implantation ionique, on pourra se reporter au livre de J. Ziegler [ZIE06].
Technologie de l’implantation ionique
Un implanteur ionique est constitué principalement d’une source d’ions, d’équipements de focalisation, d’un analyseur de masse et d’une chambre d’implantation. Dans le cadre de ce travail, nous avons utilisé un implanteur VIIsta HCP de la marque VSEA (dont l’architecture est présentée sur la Figure 4). Il s’agit d’un implanteur 300 mm fort courant dont la gamme d’énergie varie de 0,2 à 80 keV. Nous allons brièvement décrire les principales caractéristiques de cet équipement.
La source d’ions
Les ions à implanter sont créés dans la source à partir de composés gazeux ou d’éléments métalliques vaporisés ou pulvérisés. Pour l’implanteur que nous avons utilisé, il s’agit d’une source Bernas de type IHC. Dans les sources Bernas, le filament est fixé à une extrémité de la chambre et une anticathode est utilisée à l’autre extrémité. Dans une source IHC (« Indirectly Heated Cathode »), pour augmenter la durée de vie du filament, il est protégé par une cathode. Lorsque le filament soumis à un fort courant émet des électrons, une tension de quelques centaines de volts est appliquée entre ce dernier et la cathode afin d’accélérer les électrons vers celle-ci. Sous ce bombardement, la cathode atteint sa température d’émission, engendrant la formation du plasma dans la chambre.
La source de l’implanteur VIIsta est conçue pour reproduire des faisceaux de type « ruban » intenses, de l’ordre de 10 à 20 mA pour des énergies de quelques dizaines de keV. Aux basses énergies que nous avons utilisées pour cette étude (autour de 6 keV), le courant du faisceau d’hydrogène obtenu est typiquement de 5mA.
Une fois les ions créés dans la source, le faisceau d’ions est extrait par un champ électrique appliqué à la sortie de la chambre d’ionisation. Il passe ensuite dans un électro-aimant (spectromètre de masse) dont le but principal est de séparer l’espèce à implanter des impuretés présentes dans le faisceau (gaz résiduel dans le système de mise sous vide). Il a aussi pour seconde utilité d’agir comme piège pour les atomes neutres rapides formés dans la source, puisque ces derniers ne sont pas déviés par le champ magnétique. Enfin, il permet, grâce à ses propriétés de focalisation, d’agir comme les « optiques » convergentes vues auparavant.
Ligne de faisceau
Tous les composants de la ligne de faisceau sont conçus pour mettre en forme et conduire le faisceau depuis la source jusqu’au wafer à implanter. En effet, un faisceau de particules chargées tend naturellement à être divergent pour plusieurs raisons : agitation angulaire due à l’agitation thermique, force répulsive des ions… Ainsi dans le VIIsta plusieurs quadripôles, répartis après la source et après l’aimant de tri, permettent de contrôler la taille du faisceau dans les deux directions. Enfin, un deuxième aimant de déviation, placé juste avant la chambre de cible, permet de « former » le faisceau ruban à la taille voulue (35 cm de largeur environ). Il a aussi pour fonction d’empêcher les espèces neutres et les particules éventuellement produites dans la ligne de faisceau de parvenir jusqu’à la plaque.
Balayage du faisceau et chambre d’implantation
Les substrats à implanter sont ensuite balayés uniformément par le faisceau d’ions. Ce balayage peut être de trois types différents : électrostatique, mécanique ou mixte. Dans le VIIsta, le balayage est de type mécanique : la plaque est placée sur un piston qui monte et descend, lui faisant traverser le faisceau ruban autant de fois que nécessaire pour atteindre la dose programmée. Un système de dosimétrie complexe permet de garantir l’uniformité du faisceau pendant le procédé d’implantation et la dose finale implantée. La plaque est placée sur un chuck électrostatique avec un refroidissement par flux d’azote de l’arrière de la plaque. Ainsi, la température est maintenue très proche de 20°C dans nos conditions expérimentales pendant tout le procédé d’implantation.
Collage direct hydrophile
Après l’implantation, les deux plaques sont collées par collage direct hydrophile.
Principes physiques
Le phénomène de collage par adhésion moléculaire intervient lorsque deux surfaces lisses, propres et sans particule sont rapprochées à des distances de l’ordre de 10 à 100 nm. Les forces de Van der Waals qui s’établissent entre les deux surfaces sont alors suffisamment grandes pour maintenir celles-ci en contact. L’appellation « forces de Van der Waals » désigne les forces liées aux interactions électroniques entre les atomes ou les molécules de deux corps proches l’un de l’autre. Si la distance entre les deux plaques diminue encore, des interactions de type liaison hydrogène peuvent également s’établir. Ces interactions mettent en jeu des molécules polarisées présentes sur les deux surfaces en contact. Les énergies relatives à ce type de liaison varient de 10 à 40 kJ/mol, c’est-à-dire environ un ordre de grandeur au-dessus des forces de Van der Waals. Notons cependant que de telles interactions restent encore faibles par rapport aux énergies des liaisons covalentes, qui se situent entre 200 et 800 kJ/mol [ROC91]. Ces liaisons covalentes interviennent dans le cas où la distance entre les plaques est très faible.
Le collage hydrophile est basé sur la mise en contact de surfaces saturées en terminaisons –OH. C’est ce type de collage qui est utilisé par le procédé Smart CutTM.
Un modèle de collage hydrophile a été proposé par Stengl en 1989 afin d’expliquer l’évolution en température des forces et des liaisons chimiques [STE89]. A température ambiante, des molécules d’eau sont absorbées à la surface de l’oxyde sur les terminaisons –OH. Au fur et à mesure que la température augmente, des liaisons hydrogène s’établissent entre des groupes silanols (Si-OH) présents sur les deux surfaces. Finalement, pour des températures supérieures à 700°C, les complexes à base de molécules d’eau disparaissent permettant un rapprochement des surfaces (0,1-0,2 nm) par la formation des liaisons covalentes siloxanes Si-O-Si.
Technologie du collage direct hydrophile
Préparation des surfaces pour le collage
Pour un collage par adhésion moléculaire, il est donc nécessaire de maîtriser les traitements de surface afin de maximiser la densité des liaisons Si-OH. Une activation de surface est réalisée par un nettoyage chimique [RAY99]. Classiquement, un nettoyage de la surface pour éliminer les particules et les contaminants indésirables est mis en œuvre afin d’éviter la création d’éventuels défauts de collage. La contamination est, soit organique (principalement des hydrocarbures) dont l’élimination est souvent réalisée grâce au SPM (Sulphuric peroxide Mixture appelé aussi Caro) ou à l’ozone, soit particulaire dont l’élimination est efficacement réalisée grâce au bain APM (Ammonium Peroxide Mixture appelé aussi SC1). Le SC1 permet aussi d’activer les terminaisons chimiques spécifiques –OH. Dans un troisième temps, un dernier bain dit SC2 correspond à un ultime nettoyage éliminant les métaux qui se seraient potentiellement déposés sur la surface des plaques.
C’est ce type de préparation de surface qui a été réalisé sur toutes les plaques qui ont été collées dans le cadre de ce travail.
Découpe
Nous avons découpé nos plaques de 300mm en carrés de 3*3 cm² à l’aide d’une scie, après l’étape de collage, afin de pouvoir réaliser des recuits à différentes températures et différents temps pour chaque plaque.
Recuits
Les recuits ont été réalisés dans un four tubulaire sous azote (cf. Figure 5) dans une gamme de température de 300 à 500°C sans rampe de température. Les temps de recuits varient de quelques minutes à quelques heures. Le four de recuit est équipé d’un détecteur de vibration qui permet de détecter le moment où la séparation des deux plaques est obtenue.
Figure 5: Schéma du four tubulaire (AET1) utilisé pour nos recuits au CEA-LETI.
Caractérisation des échantillons
Spectrométrie de Masse par Ions Secondaires
La Spectrométrie de Masse par Ions Secondaires (SIMS) est une technique d’analyse permettant de mesurer des profils de concentration d’impuretés en fonction de la profondeur dans des régions proches de la surface de la plupart des matériaux [WIL87, BEH95]. Cette technique est destructive car elle utilise l’abrasion ionique de la matrice, résultant de l’exposition de la surface à analyser à un faisceau d’ions, généralement d’oxygène ou de césium, d’une énergie de quelques keV. Au cours de cette pulvérisation, les impuretés et les atomes constituant la matrice sont arrachés de la surface et forment de nouveaux complexes ioniques (ions secondaires) qui sont séparés en masse à l’aide d’un spectromètre de masse, puis comptés.
La vitesse d’érosion (ou taux de pulvérisation) étant connu, les profils SIMS obtenus donnent la variation de concentration d’une espèce donnée en fonction de la profondeur dans la cible. Fondamentalement, la SIMS est une technique performante pour analyser de faibles concentrations d’impuretés dans une cible homogène. La mesure de fortes concentrations d’impuretés ou d’impuretés distribuées de façon inhomogène, typique de phases précipités, est délicate. Lorsque le faisceau d’ions rencontre des microfissures ou des cloques de quelques micromètres de diamètre contenant un gaz pressurisé, de grandes quantités de ce gaz s’échappent brusquement. L’ionisation des molécules et/ou atomes constituant ce gaz est alors incomplète, voire aléatoire. Dans cette situation, la technique SIMS sous-estime systématiquement la concentration des gaz que nous souhaitons analyser [PER07].
Microscopie Confocale
En microscopie conventionnelle, l’image observée est rendue floue par la lumière émise par les plans situés en dehors du plan focal. En microscopie confocale (Figure 6), le diaphragme confocal (trou d’aiguille sur le schéma) ne laisse passer que le flux lumineux provenant du plan focal, éliminant ainsi la lumière parasite. L’image observée est alors une véritable « tranche optique » à l’intérieur de l’échantillon, un peu comme une coupe tomographique.
La microscopie confocale nécessite une lumière d’excitation particulièrement intense et focalisée. C’est pour cette raison que la plupart des microscopes confocaux utilisent un laser comme source d’excitation.
Dans le scanner, le faisceau laser est réfléchi par un miroir dichroïque puis envoyé sur des miroirs galvanométriques (miroirs de balayage) qui, en pivotant sur leur axe, permettent le balayage rapide de l’ensemble du champ. La lumière émise récupérée via l’objectif passe par, successivement, le scanner, le miroir dichroïque et le diaphragme confocal (trou d’aiguille sur le schéma), puis parvient au détecteur (photomultiplicateur). Le signal électrique émis par le photomultiplicateur est amplifié puis envoyé à l’ordinateur, où il est digitalisé, puis affiché sur le moniteur. L’ordinateur gère les miroirs de balayage, la platine galvanométrique contrôlant le déplacement en z de la platine et l’ouverture du diaphragme confocal.
Dans nos conditions expérimentales, les cloques sont de taille extrêmement réduites, et les microscopes optiques conventionnels utilisés habituellement pour ce type d’étude, ne nous permettait pas d’affirmer de façon fiable que la surface de l’échantillon présentait ou non des cloques. La résolution supérieure du microscope confocal nous a donc été d’une grande utilité pour réaliser des mesures fiables.
Microscopie Electronique en Transmission
La microscopie électronique en transmission (MET) repose sur les interactions des électrons avec la matière. L’interaction des électrons avec la matière étant très forte, il faut que l’échantillon à traverser soit très mince, de l’ordre de la centaine de nanomètres. La MET permet d’imager les défauts cristallins et les précipités, comme par exemple les platelets résultant de la précipitation d’hydrogène.
Préparation des échantillons
L’amincissement des échantillons a pour objectif d’obtenir une épaisseur dans la gamme de 50-150 nanomètres.
Nous avons préparés nos échantillons par polissage mécanique suivi d’une érosion ionique. Tout d’abord, la première face de l’échantillon est amincie par polissage mécanique à l’aide d’une polisseuse manuelle sur papier abrasif. Une fois la face bien polie (pas de rayure visible), la deuxième face est polie, plus grossièrement que la première, jusqu’à conserver environ 30-40 µm d’épaisseur à l’échantillon. Cette face est ensuite polie à l’aide d’une meuleuse afin de réaliser une concavité au centre de l’échantillon. Pour cette étape de polissage, nous utilisons un feutre sur lequel nous déposons de la pâte diamantée diluée dans un solvant. Une fois la concavité réalisée, l’échantillon est collé sur une grille en cuivre. La finition de l’amincissement est réalisée par PIPS (Precision Ion Polishing System). La concavité faite précédemment permet de focaliser le faisceau d’ion au centre de l’échantillon. Le PIPS permet de faire un trou à l’aide d’ions argon accéléré (de 2 à 6 keV) sous incidence faible (5 à 10°), si possible au centre de l’échantillon, dont les bords sont très fins. Pour nos échantillons, nous avons utilisé, sous une incidence de 7°, une énergie de 4 keV pour amincir « le plus gros » puis de 2,5 keV pour finir d’amincir et arriver jusqu’au trou afin d’éviter d’amorphiser le silicium. C’est ensuite cette zone très fine qui est observée en MET.
Observation des échantillons
Les images de microscopie électronique en transmission sont caractérisées par des contrastes d’amplitude et des contrastes de phase. De façon générale, le contraste de l’image dépend de la variation d’intensité du faisceau d’électrons à la sortie de l’échantillon. L’amplitude des faisceaux transmis et diffracté (cf. Figure 7) dépend de l’épaisseur, de la nature des atomes et de l’orientation cristalline de l’échantillon.
Nous avons utilisé deux méthodes d’imagerie au cours de ce travail : conditions en champ clair (image formée avec le faisceau transmis) à deux ondes pour mesurer l’épaisseur de l’échantillon, conditions en champ clair, hors Bragg et lentille objectif défocalisée, pour observer les platelets via leur contraste de Fresnel [CHE12]. Ces deux méthodes sont détaillées dans le chapitre 4.
Pour observer nos échantillons nous avons utilisé le MET JEOL JEM2010 (cf. Figure 8) au CEMES qui est composé d’un filament LaB6 et nous avons utilisé un porte-échantillon double-tilt (Figure 8) afin de pouvoir orienter la zone à observer.
Table des matières
Introduction générale
Chapitre 1 : Smart CutTM et couches enterrées
1. Introduction
2. La technologie Smart-CutTM
2.1. Le procédé
2.2. Avantages du procédé
3. De l’implantation à la fracture
3.1. Défauts et complexes formés lors de l’implantation
3.2. Les platelets
3.3. La théorie de la maturation d’Ostwald
3.4. Les microfissures
3.4.1. Sans raidisseur : phénomène de cloquage
3.4.2. Avec raidisseur
3.5. Fracture finale et état de la surface après la fracture
4. Hydrogène et bore
4.1. Interactions entre atomes H et B
4.2. Interactions entre atomes d’hydrogène et silicium dopé bore
4.3. Co-implantation B+H
4.4. Couche enterrée Si:B
5. Hydrogène et germanium
5.1. Couche SiGe sur substrat silicium
5.2. Couche SiGe dans du germanium
6. Bilan et objectifs
Chapitre 2 : Procédés et techniques expérimentales
1. Introduction
2. Fabrication des échantillons
2.1. Epitaxie
2.2. Oxydation thermique
2.3. Implantation ionique
2.3.1. Principe général
2.3.2. Technologie de l’implantation ionique
2.4. Collage direct hydrophile
2.4.1. Principes physiques
2.4.2. Technologie du collage direct hydrophile
2.5. Découpe
2.6. Recuits
3. Caractérisation des échantillons
3.1. Spectrométrie de Masse par Ions Secondaires
3.2. Microscopie Confocale
3.3. Microscopie Electronique en Transmission
3.3.1. Préparation des échantillons
3.3.2. Observation des échantillons
3.4. Microscope à Force Atomique
Chapitre 3 : Confinement de la fracture dans les couches enterrées Si:B et SiGe
1. Introduction
2. Etude de cloquage
2.1. Méthodologie
2.1.1. Description de l’étude de cloquage
2.1.2. Procédure d’identification des conditions favorables d’implantation et de traitement thermique
2.1.3. Analyse quantitative des images de microscopie confocale
2.2. Résultats pour la couche Si:B
2.2.1. Effet de la dose, de l’énergie d’implantation, de la température de recuit
2.2.2. Effet du dopage de bore
2.3. Résultats pour la couche SiGe
2.3.1. Effet de la dose d’hydrogène implantée
2.3.2. Effet de l’énergie d’implantation
2.3.3. Effet de la température de recuit
2.4. Conclusions de l’étude de cloquage
3. Essais de transfert
3.1. Description des essais
3.2. Tests de transfert à 500°C-1h
3.3. Cinétique de fracture
3.4. Mesures de rugosité après transfert
4. Etude du mécanisme de fracture avec une couche enterrée
4.1. Impact des couches enterrées sur le profil d’hydrogène
4.2. Impact des couches enterrées sur la localisation des défauts précurseurs de la fracture
4.2.1. Après implantation
4.2.2. Après recuit
Conclusion
Chapitre 4 : Diffusion et piégeage de l’hydrogène implanté dans des structures localement dopées de type Si/Si:B/Si
1. Introduction
2. Description des expériences
3. Analyse par Spectrométrie de Masse par Ions Secondaires
3.1. Profil après implantation
3.2. Recuits isothermes
3.3. Recuits isochrones
4. Microscopie Electronique à Transmission
4.1. Méthodes
4.1.1. Observations des platelets
4.1.2. Etude quantitative
4.2. Résultats
4.2.1. Images MET
4.2.2. Etude quantitative
4.2.3. Discussion des résultats
5. Modèle physique de diffusion et piégeage de l’hydrogène par les platelets
5.1. Pourquoi un modèle ?
5.2. Description du modèle physique
5.3. Modèle numérique
5.4. Effet des différents paramètres du modèle
5.5. Détermination du coefficient de diffusion et de l’énergie d’activation
Conclusion
Conclusion générale
Références