Sommaire: Enquête sur l’acceptabilité et la tolérance de l’ivg médicamenteuse avant et après 7 semaines d’aménorrhée
LISTE DES ILLUSTRATIONS
TABLEAUX
FIGURES
GRAPHIQUES
LISTE DES ABRÉVIATIONS
INTRODUCTION
II. Épidémiologie
2.1 Données actuelles de l’IVG en France
2.1.1 Population concernée
2.1.2 Répartition géographique
2.1.3 Répartition selon l’âge gestationnel
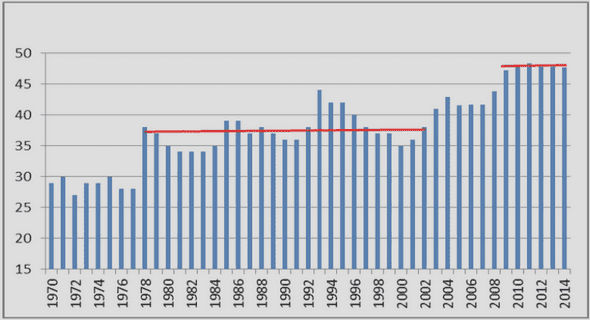
2.1.4 Évolution des méthodes
2.2 L’interruption volontaire de grossesse ailleurs
2.2.1 Dans le monde
2.2.2 En Europe
2.3 L’IVG médicamenteuse en France : États des lieux
III. Prise en charge de l’IVG médicamenteuse
3.1 Recommandations HAS 2010
3.2 Acceptabilité de l’IVG médicamenteuse
3.2.1 En France
3.2.2 Ailleurs
3.3 IVG médicamenteuse en milieu hospitalier
IV. Objectifs de l’étude
MATÉRIELS ET MÉTHODES
I. L’Étude
II. Population
2.1 Critères d’inclusion
2.2 Critères d’exclusion
2.3 Division en sous-groupes pour analyse
III. Objectifs
IV. Données recueillies
V. Questionnaire d’acceptabilité
VI. Protocoles du Planning Familial de la Pitié Salpêtrière
6.1 Protocole de l’IVG médicamenteuse à domicile
6.2 Protocole de l’IVG médicamenteuse en milieu hospitalier
VII. Analyse statistique
RÉSULTATS
I. Description de la population
1.1 Caractéristiques socio-professionnelles
1.1.1 Age
1.1.2 Situation socio-professionnelle
1.2 Antécédents personnels
1.2.1 Antécédents d’IVG
1.2.2 Parité
1.3 Age de la grossesse
II. L’IVG et ses suites
2.1 Effets secondaires observés
2.1.1 Douleur
2.1.2 Prise d’antalgiques
2.1.3 Effets secondaires observés
2.2 Métrorragies
2.3 Délai d’expulsion
III. Résultats des IVG
3.1 Perdues de vue
3.2 Résultats des IVG : succès, échecs, complications
IV. Exploitation du questionnaire d’acceptabilité
4.1 Taux de participation
4.2 Satisfaction globale sur la prise en charge
4.3 Exploitation du questionnaire
4.3.1 Pire effet secondaire
4.3.2 Douleur ressentie versus celle imaginée lors de l’IVG
4.3.3 Préférence d’une autre procédure en cas de nouvelle IVG
V. Les mineures
5.1 Caractéristiques
5.2 L’IVG et ses suites
5.3 Résultats des IVG
5.4 Exploitation du questionnaire d’acceptabilité
DISCUSSION
I. Résultats principaux
II. Validité de l’étude
2.1 Points forts de l’étude
2.2 Points faibles de l’étude
III. Données de la littérature
3.1 Caractéristiques des groupes étudiés
3.2 Tolérance et effets secondaires
3.3 Délai d’expulsion
3.4 Résultats
3.4.1 Perdues de vue
3.4.2 Efficacité de la méthode
3.5 Exploitation du questionnaire d’acceptabilité
3.6 Les mineures
CONCLUSION
BIBLIOGRAPHIE
ANNEXES
ANNEXE 1 :
Recommandations HAS 2010
« Interruption volontaire de grossesse par méthode médicamenteuse »
ANNEXE 2 :
Questionnaire d’acceptabilité de la méthode médicamenteuse dans l’IVG
RÉSUMÉ
♣ Extrait du mémoire
INTRODUCTION
I. Historique
En 1975, la loi Veil est votée à l’Assemblée Nationale avec 277 voix contre 192 et au Sénat à 185 contre 88. Elle dispose ainsi :
« La femme enceinte que son état place dans une situation de détresse peut demander à un médecin l’interruption volontaire de grossesse avant la fin de la 10 ème semaine de grossesse. » Seule la femme devient juge de sa situation.
Cette loi a pu voir le jour grâce au principe d’émancipation des femmes (droit à disposer de leur corps). Elle répond également à un objectif de santé publique, dans un pays conscient de la pratique des IVG clandestines et des complications maternelles, parfois mortelles, qui en découlent.
Cependant, une « clause de conscience » est rédigée, permettant ainsi aux professionnels de santé de refuser de pratiquer cet acte.
La loi subit une mise à l’épreuve de cinq ans, au terme de laquelle elle est réévaluée et confirmée le 31 décembre 1979 par le Parlement. Cette loi prévoit que l’IVG ne peut être pratiquée qu’exclusivement dans les hôpitaux publics et cliniques privées agrées par des professionnels de santé formés.
En 1982, la loi Roudy permet le remboursement des frais liés à l’avortement à hauteur de 80%.
En 1988, alors que la mifepristone (RU486), qui sera commercialisée sous le nom de Mifegyne, obtient l’Autorisation de Mise sur le Marché en France, le laboratoire est contraint, sous peine de boycott, de la retirer avant sa commercialisation effective. C’est le Ministre de la Santé, Claude Evin, qui la réhabilite.
En 1989 la France devient le premier pays occidental à utiliser la Mifegyne (après la Chine en 1987), offrant ainsi aux femmes une alternative sûre et efficace à l’avortement chirurgical.
Ainsi, selon le terme de la grossesse, deux méthodes d’interruption volontaire de grossesse sont possibles pour les femmes : la méthode dite « médicamenteuse » consistant en la prise successive de deux médicaments, et la méthode dite « chirurgicale », sous anesthésie locale ou générale, par aspiration endo-utérine.
En 1993, la loi Neiertz punit les délits d’entrave à l’IVG (jusque 2 ans de prison ferme et 30000 francs d’amende).
La loi Guigou-Aubry du 4 juillet 2001 est en faveur d’une facilitation de l’accès à l’avortement, notamment suite aux difficultés énoncées dans le rapport Nisand en 1999.
Ses principales modifications sont :
– L’entretien pré-IVG devient facultatif pour les femmes majeures mais reste obligatoire pour les mineures
– Le délai légal est allongé de deux semaines, porté à 12 semaines de grossesse ou 14 semaines d’aménorrhée
– La prescription du RU 486 par les médecins de ville est autorisée sous certaines conditions
– L’autorisation parentale, pour les mineures, n’est plus obligatoire ; la présence d’un adulte référent est requise
– Délivrance anonyme et gratuite d’une contraception d’urgence
– Les médecins libéraux peuvent prescrire une contraception à une mineure sans autorisation parentale
– Les femmes étrangères ne doivent plus justifier d’un titre de séjour pour avoir accès à l’IVG
Les décrets permettant l’application de la loi de juillet 2001 sur la réalisation des IVG hors établissements de santé ne sont parus qu’en 2004.
Les médecins de ville peuvent proposer aux femmes une IVG médicamenteuse, dans le cadre d’un réseau ville /hôpital ; l’hôpital restant le recours en cas de complications ou d’échecs.
En 2007, l’agence européenne du médicament modifie l’AMM de la Mifegyne et l’autorise jusque 7 semaines d’aménorrhée en ville, et jusque 9 semaines d’aménorrhée avec une courte surveillance hospitalière.
……….