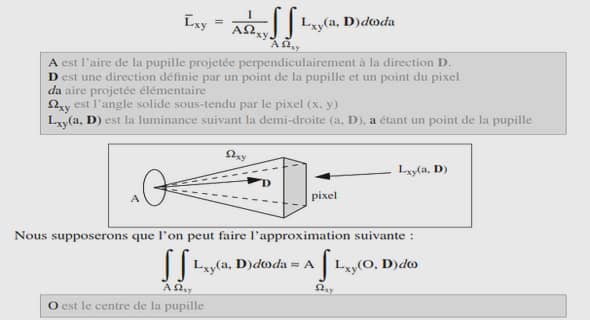
Les colorants
Définition Depuis la préhistoire, l’homme a été intéressé par les colorants caractérisés par l’application de teintures naturelles pour les fourrures et le textile. Ces premières teintures étaient principalement d’origine végétale, ainsi que d’origine animale. Parmi ceux-ci, on cite l’Indigo naturel obtenu de la plante Indigofera tinctoria, le pourpre Tyrien extrait de la glande d’un escargot violet développé par les Phéniciens. Les milliers d’années de développement ont mené à des processus compliqués de teinture. En 1856, William H. Perkin a réussi à obtenir une teinture qu’il a nommé Partie I : Synthèse bibliographique Chapitre I : Les colorants -9- Mauvéine. Ceci a été réalisé par l’oxydation d’un mélange de bases d’aniline pour produire une teinture cationique violette. La nuance violette brillante sur la soie a immédiatement attiré l’attention et a stimulé d’autres chimistes pour effectuer des expériences semblables. Des découvertes semblables ont été réalisées, en 1859 Verguin a découvert la fuchsine, tandis que Griess a découvert les composés diazoïques qui ont mené au développement de la grande classe actuelle de teintures synthétiques, à savoir les composés azoïques. La première vraie teinture d’azo, Bismark le Brun, a été développée par Martius en 1863 [2]. Le dictionnaire Larousse définit un colorant comme étant une substance colorée, naturelle ou synthétique, qui mise en contact avec un support, dans des conditions appropriées, se fixe sur ce dernier de façon durable en lui communiquant une certaine couleur [3]. Les matières colorantes se caractérisent par leur capacité à absorber les rayonnements lumineux dans le spectre visible (de 400 à 700 nm). Tous les composés répondant à cette définition se différencient par leur structure chimique, organique ou inorganique, ou par leur origine, naturelle ou synthétique [4]. Les doubles liaisons, qui permettent l’absorption de la lumière dans le domaine du visible ou de l’ultraviolet, sont des groupes chromophores (du grec khrôma : couleur et phero : je porte). La présence de substituants peut modifier la longueur d’onde d’absorption. Le déplacement de l’absorption vers les plus grandes longueurs d’onde dans le domaine visible est dû notamment à la présence de certains groupes auxochromes (du grec auxein : accroître) couplés aux groupes chromophores illustrés sur le Tableau I.1. Les couleurs de la nature sont dues à l’absorption sélective, par des molécules, de certaines radiations du spectre visible de la lumière blanche. Plus une molécule contient de doubles liaisons conjuguées, plus la longueur d’onde de la lumière absorbée est grande [5].
Classification des colorants
La classification des colorants la plus utilisée est celle du Colour Index qui répertorie la majorité des colorants mis sur le marché. Elle comprend deux systèmes de classification complémentaires : l’un utilise l’appellation usuelle (ou reference number) basé sur le mode d’utilisation et d’application du colorant, tandis que l’autre utilise la structure chimique (numéros de Colour index). a) Classification technologique La classification technologique permet à l’utilisateur de connaitre le mode d’application du colorant (ou appellation usuelle) et donc ses domaines d’utilisation, ses propriétés (solubilité, affinité pour tel type de fibres ou matériaux, nature de la fixation…). La confidentialité sur la composition chimique peut être préservée. Elle comprend trois éléments : Le nom générique de la classe d’application ; La couleur ; Le numéro d’ordre chronologique d’inscription au Coulor Index. Le Disperse Blue 106, par exemple, est un colorant de couleur bleue, de la classe Disperse, inséré en 106e position parmi les colorants bleus Disperse [6]. Colorants dispersés Ces teintures sont fréquemment insolubles ou peu solubles avec modération dans l’eau, de caractère non-ionique et sont appliquées aux fibres hydrophobes dans une dispersion aqueuse. Elles sont principalement utilisées pour la coloration du polyester, du nylon et de la cellulose, des fibres d’acétate et acryliques, bien que certaines de leurs propriétés de stabilité humide sur ces substrats soient faibles [2]. Colorants anioniques ou acides Ces colorants peuvent être appliqués au nylon, la laine ou la soie dans la gamme de pH de 3.0 à 7.0. L’affinité teinture-fibre résulte des forces électrostatiques ion-ion, par exemple, dans le nylon entre le groupe amino, qui est protoné dans des conditions acides et la teinture anionique. La solubilité de ces colorants dans l’eau est due à la présence du groupe sulfonates. Ces colorants font partie de la famille des azoïques, une classe chimique qui compte parmi les plus larges [2]. Colorants cationiques ou basiques Ces teintures sont d’habitude appliquées à l’acrylique, papier et nylon, mais peuvent aussi trouver une utilisation dans des substrats de polyester modifiés. Les colorants basiques sont hydrosolubles et produisent des cations colorés dans la solution ; ces cations sont attirés électro-statiquement aux substrats avec une charge négative. Des teintures cationiques peuvent avoir une charge positive localisée sur un groupe d’ammonium (ces teintures sont caractérisées par une haute force tinctoriale), ou il peut être distribué comme une charge délocalisée sur le cation comme trouvé dans beaucoup de triarylméthane, xanthènes et des teintures d’acridine [2]. Colorants réactifs Ils établissent une liaison de covalence avec la fibre. Le but de cette technique est de rendre provisoirement soluble certains colorants afin de faciliter leur diffusion dans le textile, puis les insolubiliser au sein du matériau. Les colorations ainsi obtenues présentent une très haute tenue au lavage. Ils sont utilisés pour le coton et les fibres polyamides. Ce sont des colorants azoïques sur lesquels la présence de groupements sulfoniques et carboxyliques confère l’hydrosolubilité nécessaire [7]. b) Classification chimique Les colorants dont la formule chimique est divulguée sont également classés dans le Colour Index par un numéro de Colour Index : « CI number » . À partir de la classification chimique du CI, Cavalier et al. On classé les colorants en 17 rubriques [8]. On citera dans ce qui suit les familles chimiques les plus utilisées dans le domaine textile. Les colorants azoïques Ils sont caractérisés par un ou plusieurs groupements chromophores azo (–N=N–), permettant l’association d’amines aromatiques ou de molécules aromatiques hydroxylées. Ils représentent environ 70% du marché des colorants avec plus de 100000 teintes. On trouve dans cette classe, d’autres substances telles que des pigments insolubles dans l’eau, des azoïques type solvants, des colorants basiques, Partie I : Synthèse bibliographique Chapitre I : Les colorants -12- acides, des azoïques de type Disperse qui sont très utilisés comme colorants textiles et comprennent les allergènes le plus souvent incriminés dans l’exploration des eczémas de contact aux colorants textiles par tests épicutanés. Les colorants azoïques forment une gamme étendue de nuances (du jaune au bleu, au vert et même au noir) [8]. Colorants anthraquinoniques C’est la deuxième classe de colorant textiles la plus utilisée (après les colorants azoïques). Ils représentent 20 à 25 % du marché des colorants textiles. La structure de base est celle de l’anthraquinone, ils sont caractérisés par le groupement chromophore C O [8]. Colorants indigoïdes Ils tirent leur appellation de l’indigo, déjà utilisé par les Egyptiens. L’indigo est un des plus anciens colorant connus. Utilisés pour la teinture des textiles et sont également appelés « vat pigments» (ou pigments de cuve), car c’est dans la cuve que s’effectue la réduction qui permet la solubilisation de l’indigo et donc sa fixation sur la fibre. Dans un second temps, l’indigo se réoxyde à l’air. De façon générale, ces colorants résistent au lavage, moins à la lumière. L’industrie du jean a beaucoup favorisé son utilisation [7]. Les dérivés du phénylméthane Les colorants du diphénylméthane et du triphénylméthane et leurs dérivés hétérocycliques constituent la plus ancienne classe de colorants synthétiques. Ils ont conservé une certaine valeur commerciale car ils permettent de couvrir la totalité de la gamme de nuances, du jaune au bleu en passant par le rouge et même le vert. Ils sont formés de deux ou trois noyaux aromatiques reliés entre eux par un atome de carbone. Le triphénylméthane permet de réaliser la synthèse de colorants basiques (vert de malachite, violet cristallisé…), cette classe comprend des colorants cationiques, acides et à mordants, en général rouges, violets, bleus ou verts. Ces colorants ont été et sont parfois encore utilisés comme substances thérapeutiques pour leurs vertus antiseptiques, fongicides et bactéricides [7].