TROUBLES METABOLIQUES CHEZ LES PATIENTS
SOUS TRAITEMENT ANTIRETROVIRAL
RAPPEL SUR VIH
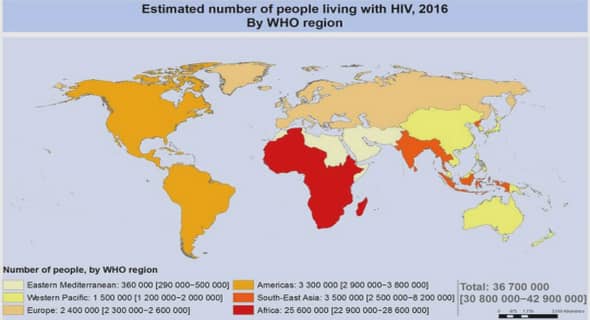
. Dans le monde En 2015, l’ONUSIDA estimait à 36,9 millions de personnes vivaient avec le VIH comme le montre la figure 1.Le nombre des personnes vivant avec le VIH continue d’augmenter, en grande partie du fait que davantage de personnes dans le monde ont accès à la thérapie antirétrovirale et vivent ainsi plus longtemps, et en meilleure santé. En juin 2015, 15,8 millions de personnes avaient accès au traitement. Parallèlement, bien que les nouvelles infections à VIH aient diminué, un nombre inacceptablement élevé de nouvelles infections à VIH et de décès liés au sida surviennent encore chaque année. En 2015, environ 2 millions de personnes ont été nouvellement infectées par le VIH et 1,2 million de personnes sont décédées de maladies liées au sida.
En Afrique Subsaharienne
L’épidémie du VIH présente de grandes variations selon les zones géographiques. Les pays d’Afrique Australe et d’Afrique de l’Est constituent l’épicentre de la pandémie dans le monde. En Afrique subsaharienne, le nombre de personnes infectées par le VIH est estimé à 25 millions, ce qui représente 70% des personnes vivant avec le VIH dans le monde. Le nombre de nouvelles infections est passé de 2,3 à 1,4 millions entre 2000 et 2014. Une baisse d’incidence de plus 50% a été notée dans certains pays tels que le Burkina Faso, le Ghana, la Zambie et le Zimbabwe. Malgré ces progrès, 70% des nouvelles infections de 2014 ont été enregistrées en Afrique subsaharienne, soulignant ainsi la nécessité de renforcer les efforts de prévention du VIH dans la région. Le nombre de décès liés au SIDA a diminué de 34 % de 2000 (1,2 millions) à 2014 (790 000) [1]. 7 Figure 2 : La prévalence du VIH en Afrique sub-saharienne et dans le monde [1]. 8 1.3. AU SENEGAL La situation du VIH au Sénégal est caractérisée par une épidémie stable avec une séroprévalence faible 0,5 % [4].Elle est basse dans la population générale (0,7% / EDS5 2011) et élevée chez les populations clés les plus exposées au risque du VIH comme les PS (18,5% / ENSC 2006), les MSM (21,8% / ELIHoS 2007) et de 9,4% chez les injecteurs de drogues intraveineuses (UDI) (EDS 5, 2010- 2011).
Classification des rétrovirus
Les virus de l’immunodéficience humaine (VIH) appartiennent à la famille des rétroviridaes, notamment à la sous famille des lentivirus. Ils sont définis essentiellement par leur mode de réplication. Deux types de virus ont été identifiés à ce jour : le VIH-1 répandu, sur l’ensemble des continents, et le VIH2 présent surtout en Afrique de l’Ouest. 2.2. Aspects structuraux Les rétrovirus se présentent sous forme de particules sphériques d’un diamètre de 80 à 100 nm. Ces particules sont constituées d’une enveloppe externe d’origine extracellulaire dans laquelle sont insérées des glycoprotéines d’enveloppe du virus. Cette enveloppe, tapissée à l’intérieur de la particule virale par une matrice, entoure la capside virale centrale ou excentrée, qui contient le génome viral, la nucléocapside et les enzymes nécessaires à la réplication du virus. Les particules virales sont libérées de la cellule dans laquelle elles se répliquent par un processus de bourgeonnement. Le génome de ces virus, constitué de deux copies d’ARN simples brins de polarité positive, de haut poids moléculaire est en effet transcrit en ADN bicatenaire grâce à une enzyme contenue dans le virion et caractéristique de cette famille : la transcriptase inverse. 10 Figure 3 : Structure du VIH
Interactions VIH-cellules et conséquences sur la physiopathologie de la maladie
Les lymphocytes T CD4+, auxiliaires spécifiques du VIH, sont capables de produire IL2 et IF gamma en réponse au VIH. Leur rôle est déterminant dans la primo infection traitée précocement par les ARV, mais aussi chez les sujets asymptomatiques à long terme. Cette réponse spécifique anti – VIH est responsable de la progression extrêmement lente de l’infection. Leurs cibles principales sont les protéines de capside, p24, p17 et gp120. Les lymphocytes T cytotoxiques au VIH représentent l’un des principaux mécanismes effecteurs impliqués dans la lutte antivirale. Ces cellules CD8+ sont retrouvées dans le sang périphérique et au niveau des lymphocytes infiltrant les organes infectés. Elles reconnaissent de multiples déterminants antigéniques appelés « épitopes » dans les protéines du VIH. Il s’agit essentiellement des protéines structurales de l’enveloppe et de la capside, la transcriptase inverse et des protéines de régulation. En effet, les lymphocytes CD8+ interviennent dans le contrôle négatif de la réplication virale par la production de molécules dites « suppressives ». La diminution de la charge virale associée à la latence clinique observée au cours de l’infection à VIH correspond de manière temporaire au développement d’une réponse lymphocytaire T cytotoxique spécifique
Cycle de réplication du VIH dans la cellule hôte
Sa connaissance est essentielle à la compréhension de la physiopathologie de l’infection à VIH et, surtout, chacune de ces étapes constituent une cible potentielle pour une thérapeutique antirétrovirale [7]. La figure 4 illustre les différentes étapes du cycle de réplication du VIH dans la cellule hôte que sont : – L’absorption et à la pénétration du virus dans la cellule ; – La seconde étape comporte plusieurs phases : – La synthèse d’ADN bi caténaire – L’import nucléaire et l’intégration de l’ADN: – la transcription du provirus – la synthèse des protéines virales à partir des ARN messagers viraux – l’assemblage de poly protéinés virales et de l’encapsidation de l’ARN viral.Figure 4: Cycle de réplication du VIH dans la cellule hôte
Cellules cibles des virus VIH
Les cellules sensibles à l’infection à VIH [7] sont la sous population de lymphocytes T CD4+ help er (ou auxiliaire) en particulier les cellules T CD4+ mémoires, mais aussi les macrophages, ou d’autres cellules telles les cellules dendritiques et les cellules de Langerhans du derme, ainsi que les cellules micro gliales du cerveau. 2.4. Eléments d’histoire naturelle L’évolution de l’infection à VIH peut être divisée en trois phases : – La phase aiguë ou primo-infection qui dure quelques semaines, 13 – La phase chronique, qui dure plusieurs années, caractérisée par une latence clinique mais sans latence virologique, – La phase finale symptomatique, qui dure de quelques mois à peu d’années.
Diagnostic de l’infection à VIH
Manifestations cliniques
Phase aiguë ou primo-infection Les premiers symptômes surviennent le plus souvent 10 à 15 jours après la contamination (extrêmes : 5-30 jours) [7]. Ils sont peu spécifiques
Signes fonctionnels
Il s’agit de la dysphagie, des céphalées, des myalgies, de l’asthénie et de l’amaigrissement [10,11,9]. 2.5.1.1.2. Signes physiques Il s’agit : D’une fièvre présente dans 90% des cas ; De signes cutanés- muqueux : La pharyngite est plus fréquente. Elle survient dans deux tiers des cas et réalise une angine érythémateuse, érythémateux-pultacée. Une éruption cutanée de type maculopapuleux survient dans la moitié des cas, quelques jours après le début de la fièvre. D’atteintes ganglionnaires : des adénopathies superficielles, apparaissent dans plus de la moitié des cas, de façon retardée, au moment où le syndrome grippal commence à disparaître. Il s’agit en général d’adénopathies multiples, siégeant principalement dans les aires cervicales, axillaires et inguinales. Elles régressent lentement, en plusieurs semaines; certaines peuvent persister pendant plusieurs mois. Des signes digestifs: 14 Ils sont plus rares mais plus spécifiques dans la mesure où ils ne sont pas décrits dans les autres causes de syndrome mononucléosique. Il s’agit principalement de la diarrhée, parfois associée à des douleurs abdominales. Une candidose orale peut également survenir à cette occasion. Des signes neurologiques : Ils sont rapportés dans 10% des cas. Il peut s’agir de méningo-encéphalites, de méningites lymphocytaires isolées ou d’atteintes neurologiques périphériques (mononévrite, ou polyradiculonévrite). La paralysie faciale est la mononévrite la plus fréquente. La médiane de la durée de la primo-infection est de deux semaines [9] mais certains symptômes du syndrome de primo-infection à VIH peuvent persister plusieurs semaines.
INTRODUCTION |